
文丨青衫人
具有硫酸化多糖衍生共聚物的热响应水凝胶是一种具有广泛应用潜力的智能材料。
通过调控碳水化合物主链的结构和性质,可以对水凝胶的响应性能和机械性能进行调节,从而实现更广泛的应用领域。
硫酸化多糖衍生共聚物是一类由硫酸化多糖和共聚物组成的材料。

硫酸化多糖是一种天然的多糖,具有良好的生物相容性和生物可降解性。共聚物可以提供材料的稳定性和机械性能。通过将这两种组分进行共聚,可以获得具有独特性能的热响应水凝胶。
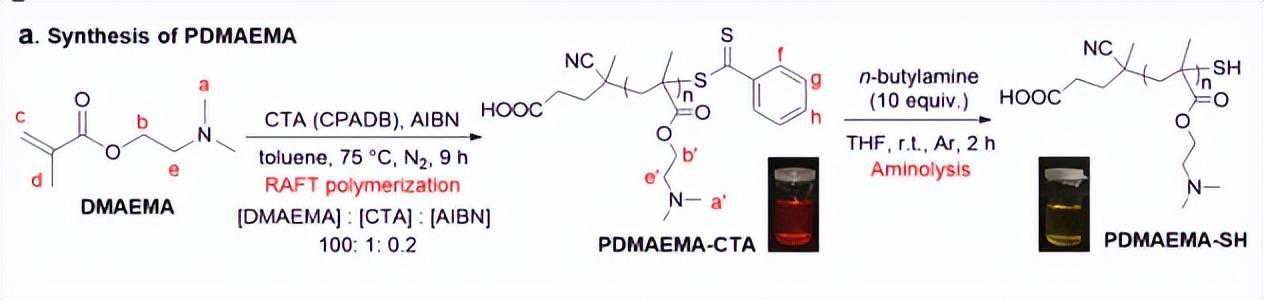
将单体DMAEMA(4.716g,30mmol,100当量)、链转移剂氰基泛酸二硫代苯甲酸酯(CPADB)(83.81mg,0.3mmol,1.0当量)、引发剂AIBN(9.85mg,0.06mmol,0.2当量)在甲苯(15mL)中的混合物装入Schlenk管中。

通过三个冷冻-抽空-解冻循环对混合物进行脱气。然后,将管密封并在氩气气氛下在75℃的油浴中加热。聚合6小时后,通过在冰水中冷却并暴露于空气来猝灭反应。
通过在冷正己烷(150mL)中沉淀来分离PDMAEMA-CTA。为了充分除去单体,将聚合物重新溶解在氯仿中并从冷n中沉淀出来,己烷再清洗两次。
收集得到的黄色油状沉淀,为带有链转移剂残留的低聚物PDMAEMA,命名为PDMAEMA-CTA,真空干燥过夜,收率29wt%。

首先,将纤维素(2.5克,15.4毫摩尔AGU,1.0当量)悬浮在500毫升烧瓶中的无水DMF(125毫升)中。将混合物在室温下搅拌超过14小时。
然后,在冰水浴和氩气气氛下,在5分钟内将氯硫酸(6.171mL,92.8mmol,6.0当量)滴加到DMF(25mL)中,然后缓慢加入乙酸酐(5.835mL,61.7mmol,4.0当量)来制备硫酸化试剂。
随后,在冷却下将硫酸化试剂滴加到纤维素悬浮液中。充入氩气并密封后,将烧瓶置于40℃油浴中5小时。此后,将混合物倒入无水乙酸钠的饱和乙醇溶液(600mL)中。
通过离心并用125mL4%乙酸钠乙醇溶液洗涤,然后用1M氢氧化钠乙醇溶液脱乙酰基15小时获得沉淀。再次离心后,将沉淀物溶解在去离子水(DI-水)中过夜。
用乙酸/乙醇(50/50,m/m)将pH值调节至8.0,并将溶液过滤。将产物用超纯水透析(在MWCO=3.5kDa的透析膜中)1周,然后冻干成干品。
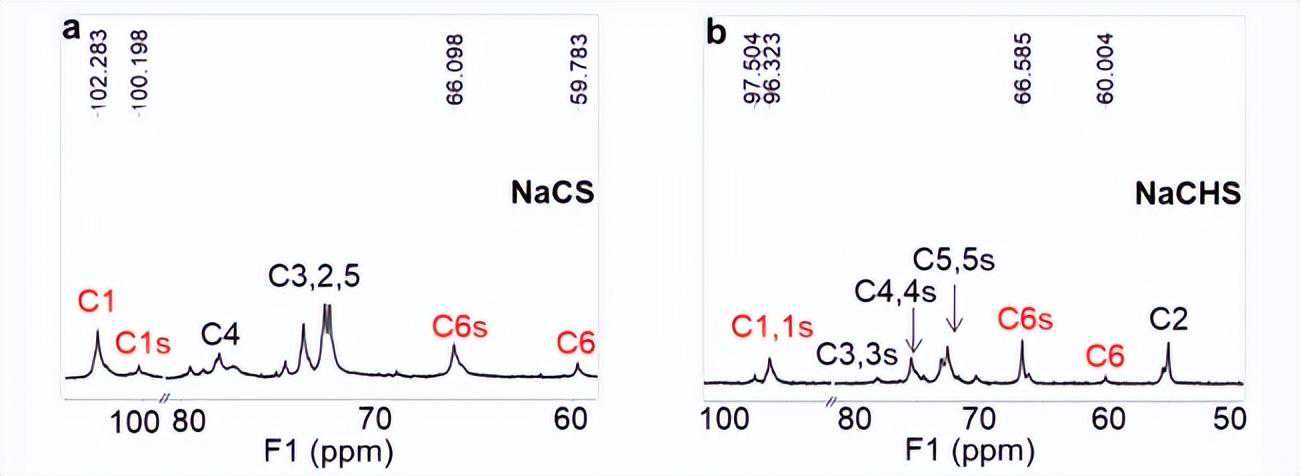
13CNMR(125MHz,D2O):δ102.28(C1)、100.20(C1S)、78.07(C4)、74.27–71.76(C3、C2、C5)、66.10(C6S)、59.78(C6)。
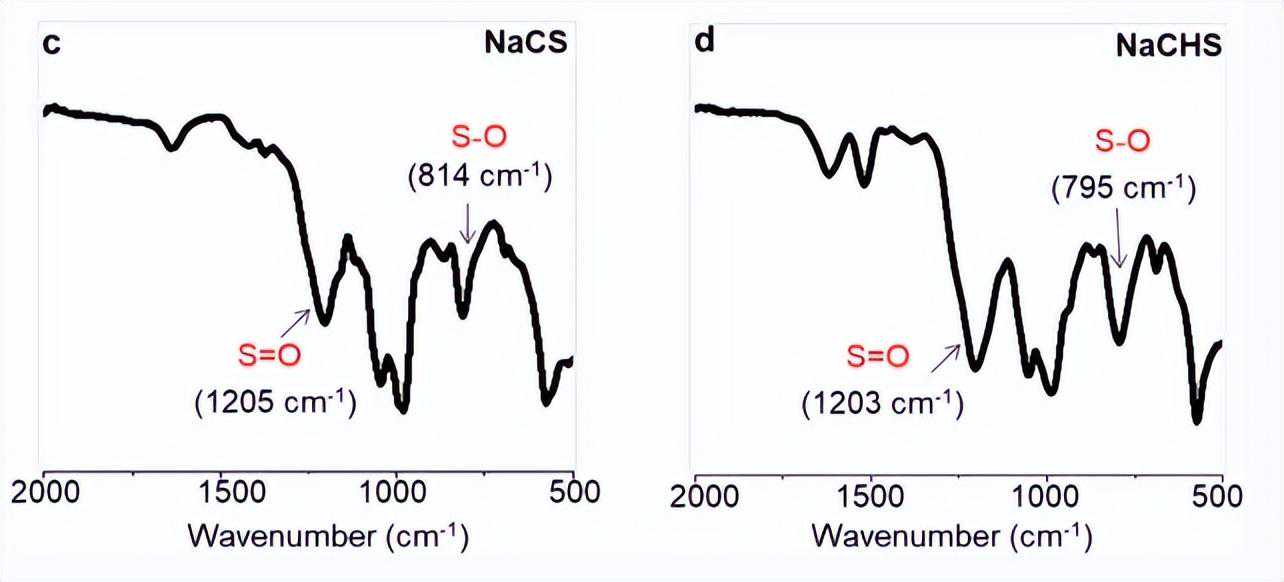
FT-IR(ATR),单位cm−1:ν̃=1205(S=O),814(S–O),硫酸根的取代度为DSS=1.0。DS的计算方法和元素分析结果的详细信息可以在支持信息中找到。

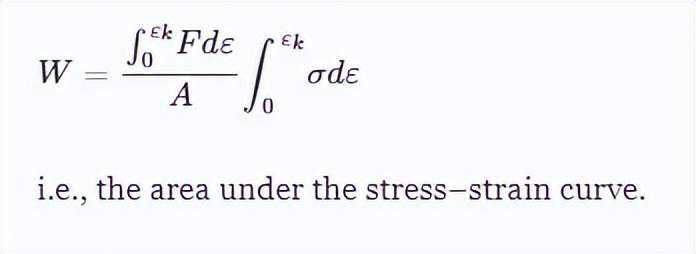
将壳聚糖(1.0g,6.2mmol单位,1.0当量)在搅拌下于1小时内溶解于甲酸(20mL)中,然后加入无水DMF(156mL)并搅拌2小时。
通过在冷却和氩气氛下,在10分钟内将氯硫酸(2.476mL,37.2mmol)缓慢滴入DMF(10mL)中来制备硫酸化试剂。
然后在30分钟内将硫酸化试剂滴加到壳聚糖溶液中,并将混合物在50℃下保持5小时。
在指定的反应时间后,将黄色溶液倒入饱和无水乙酸钠乙醇溶液(600mL)中。用乙醇/水溶液(4/1,v/v)洗涤沉淀物并在搅拌下溶解在去离子水中过夜。
用0.5M氢氧化钠溶液将pH值调节至7.5。将产物用超纯水透析(在MWCO=3.5kDa的透析膜中)1周,然后冻干成干品。
13CNMR(125MHz,D2O)δ97.50(C1)、96.32(C1S)、78.11(C3,3S)、75.88–73.85(C4,4S)、72.72(C5,5S)、66.58(C6s)、60.00(C6)、54.98(C2)。
FT-IR(ATR),单位cm−1:ν̃=1203(S=O),795(S–O)。硫酸根的取代度为DSS=1.67,DS的计算方法和元素分析结果的详细信息可以在支持信息中找到。
水凝胶的制备:
我们使用聚丙烯酰胺水凝胶作为基材,具有高透明度和可比的机械性能。同时,P-CS或P-CHS被添加到水凝胶网络内部并作为刺激响应单元。通常,水凝胶的构建如下。
CS水凝胶:单体丙烯酰胺(0.14g,2mmol)、交联剂N,N'-亚甲基双丙烯酰胺(MBA,1.4mg,0.009mmol)、催化剂N,N,N',N'-四甲基乙二胺(TEMED,10μL)和P-CS(20mg)在1mL去离子水(–6.4,3次测试)并提前在冰箱(0℃)中冷却30分钟。
之后,加入过硫酸铵(APS,1M,8μL)作为引发剂,并将混合物快速转移至模具中。水凝胶迅速制备10分钟,并储存在饱和蒸汽环境下以供后续测量。
CHS水凝胶:将单体丙烯酰胺(0.14g,2mmol)、交联剂MBA(1.4mg,0.009mmol)、催化剂TEMED(10μL)和P-CHS(20mg)的混合物在1mL去离子水(,3次测试)中混合,并提前在冰箱(0℃)中冷却30分钟。
之后,添加APS(1M,8μL)作为引发剂,并将混合物快速转移至模具中。水凝胶迅速制备10分钟,并储存在饱和蒸汽环境下以供后续测量。
将纯聚丙烯酰胺水凝胶设置为对照水凝胶。除了不存在刺激响应单元外,前体溶液的组成与P-CS或P-CHS水凝胶中的相同。

紫外可见测量在Cary300紫外可见分光光度计上进行。采用波长600nm处的透过率来表征薄膜的透明度。
核磁共振波谱1HNMR和13CNMR谱是在BrukerAvanceIII500MHz光谱仪上在氘化溶剂中于25°C下获得的。
1HNMR谱图的扫描次数为150次,13CNMR谱图的扫描次数累计高达15,000次。报告相对于溶剂峰的化学位移。
室温下在AlphaFT-IR光谱仪上记录FT-IR光谱。使用在4000和500cm-1之间以4cm-1的分辨率测量所有样品并累积24次扫描。
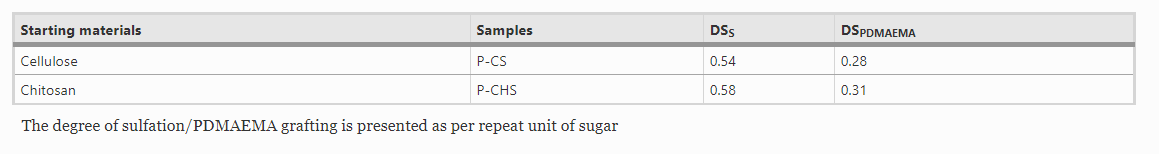
测定合成的PDMAEMA低聚物的分子量分布,THF用作洗脱液,甲苯(99.7%,干燥)作为内标(流速1.0mL∙min-1)。该系统用聚苯乙烯标准品进行校准。
水凝胶的力学性能:
使用传感器的Z3微拉伸试验机测定水凝胶的机械性能。十字头速度为6mm/min,变形速度为2.5%s-1。
弹性模量(E)计算为应变范围0至100%内的标称压缩应力-应变曲线的斜率。
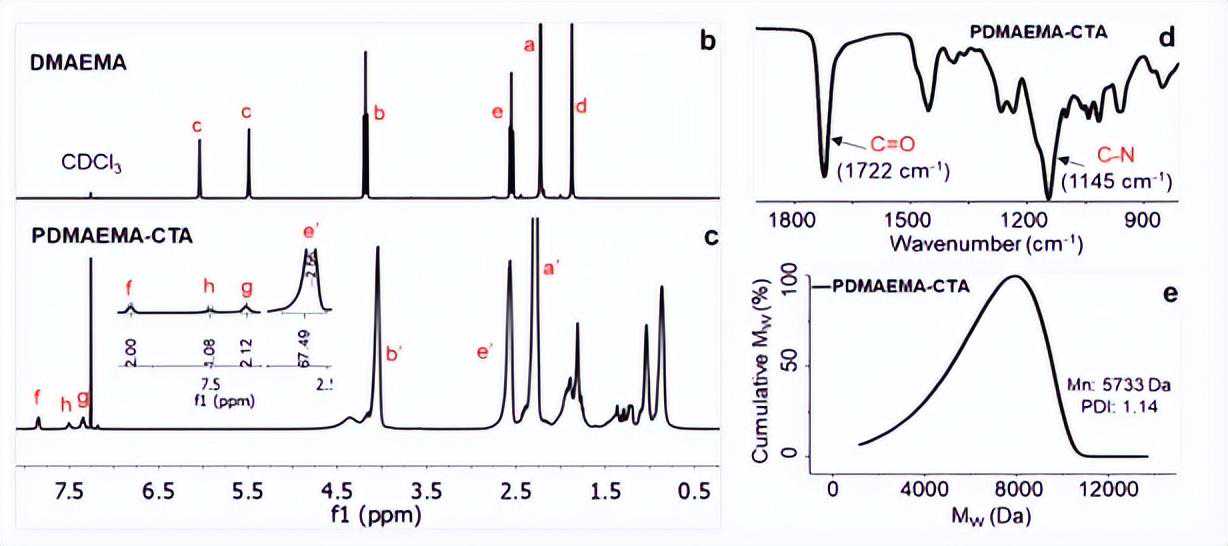
为了制备水凝胶,首先合成聚合物链段。通过可逆加成-断裂链转移(RAFT)聚合合成了含有链转移剂的PDMAEMA(PDMAEMA-CTA)。所得PEMAEMA-CTA(Mn:5733Da和Mw:6560Da,多分散指数(PDI=Mw/Mn):1.14)通过凝胶渗透色谱、核磁共振光谱和变换红外光谱分析进一步验证。
红色PDMAEMA-CTA在THF溶液中氨解,得到黄色PDMAEMA-SH。
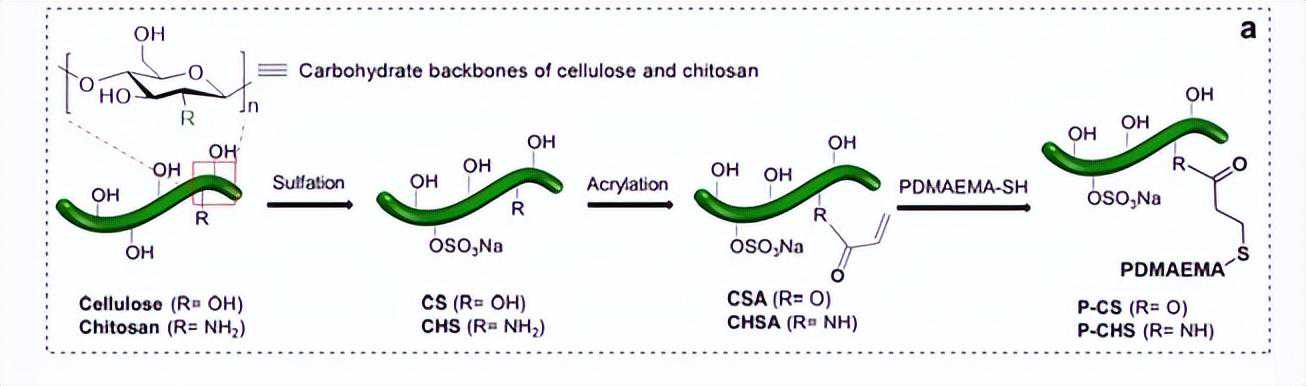
同时,按照先前的方法,通过纤维素和壳聚糖的硫酸化制备了硫酸纤维素(CS)和硫酸壳聚糖(CHS)。
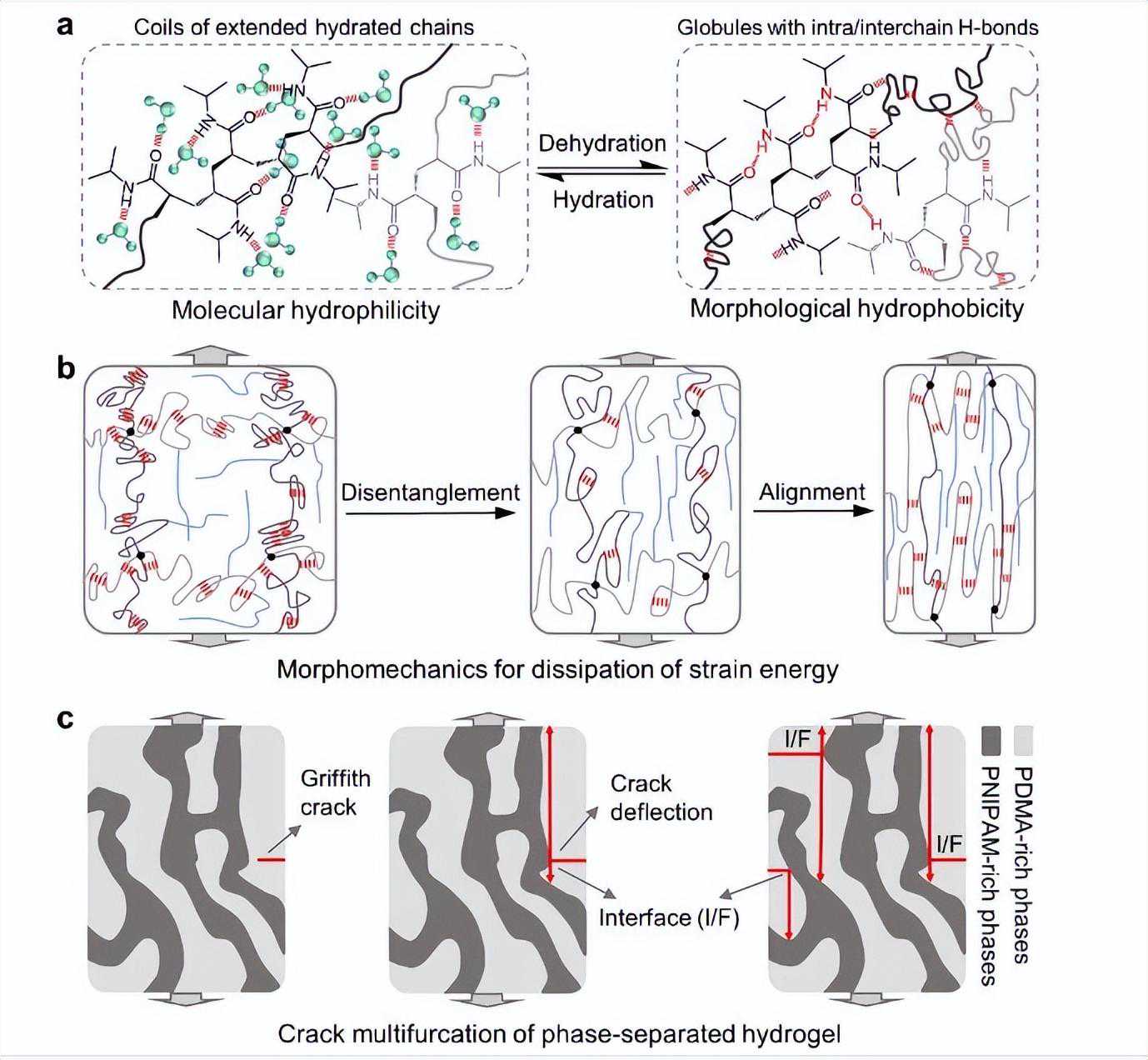
CS和CHS的结构通过元素分析、13CNMR和FT-IR分析进行了表征。
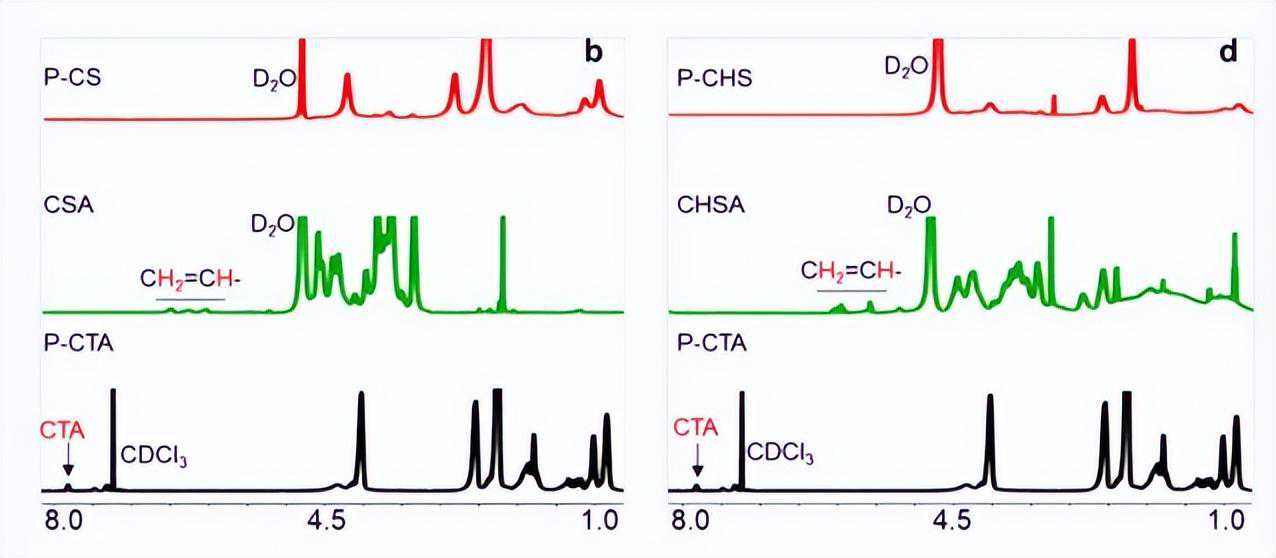
所得CS和CHS进一步改性为硫酸丙烯酸纤维素(CSA)和硫酸丙烯酸壳聚糖(CHSA),并通过1H/13CNMR、元素分析和FT-IR分析进行验证。
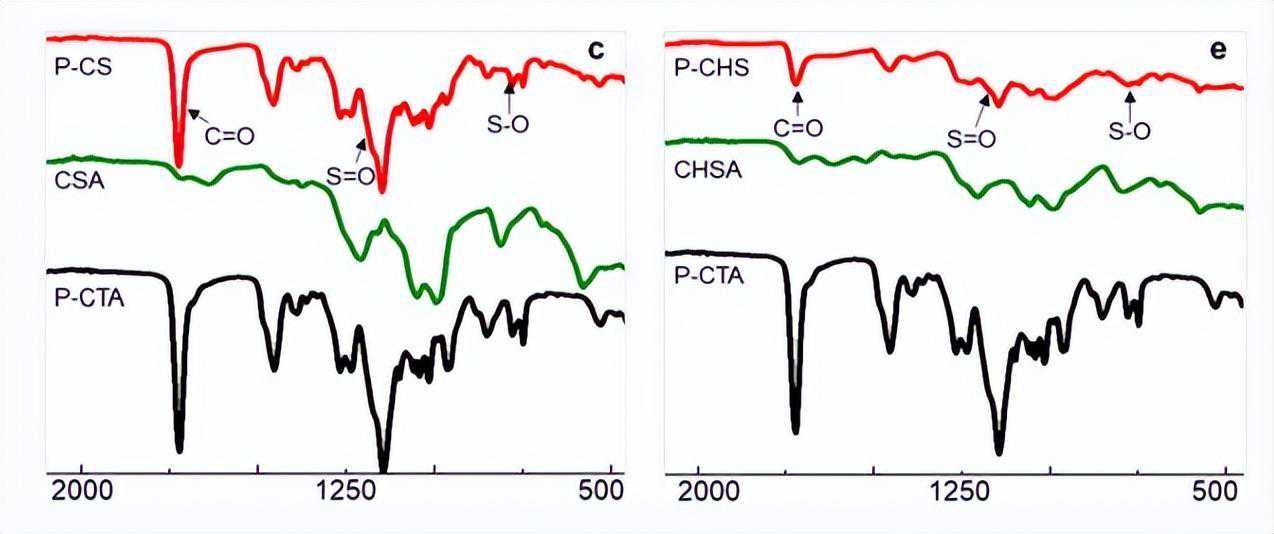
CS和P-CHS的制备通过元素分析、NMR和FT-IR光谱证实。首先,反应后CSA中丙烯酸酯基团的1HNMR信号消失,而CSA和P-CTA脂肪族区域的信号可以在P-CS的1HNMR谱中找到。
此外,C=O、S=O和S-O键的特征信号在P-CS的FT-IR光谱中可见。P-CHS还通过1HNMR和FT-IR光谱进行了验证。
根据元素分析和13CNMR谱的结果,确定P-CS的硫酸基取代度(DSS)和PDMAEMA基取代度(DSPDMAEMA)分别为0.54和0.28。使用相同的计算方法,得到具有DSS(0.57)和DSPDMAEMA(0.31)的P-CHS。
在制备水凝胶之前,利用动态光散射研究了P-CS和P-CHS溶液的热响应特性。P-CS和P-CHS的下临界溶解温度(LCST)可以在粒径曲线中确定。

与P-CHS在40°C的浊点相比,P-CS在39°C的浊点略低。随着温度升高至45℃,P-CS的流体动力学半径(Rh)明显增加,而P-CHS的Rh略有增加。
在制备这些多糖衍生物后,通过聚合含有P-CS、单体丙烯酰胺、引发剂APS、催化剂TEMED和交联剂MBA的水溶液,首次制备了离子型P-CS水凝胶。
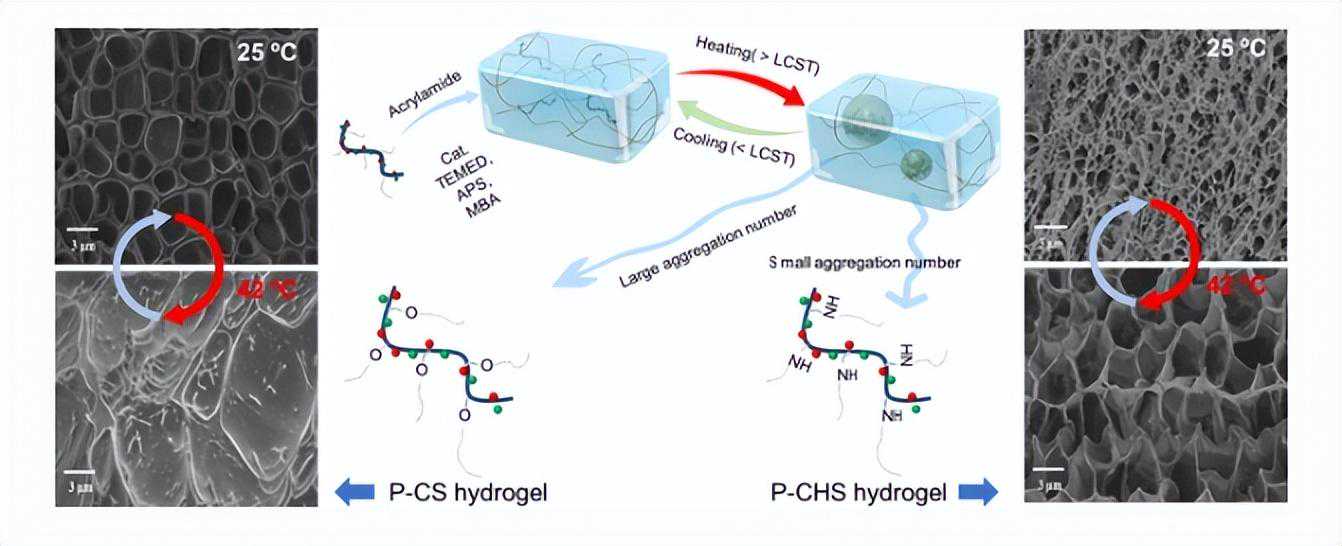
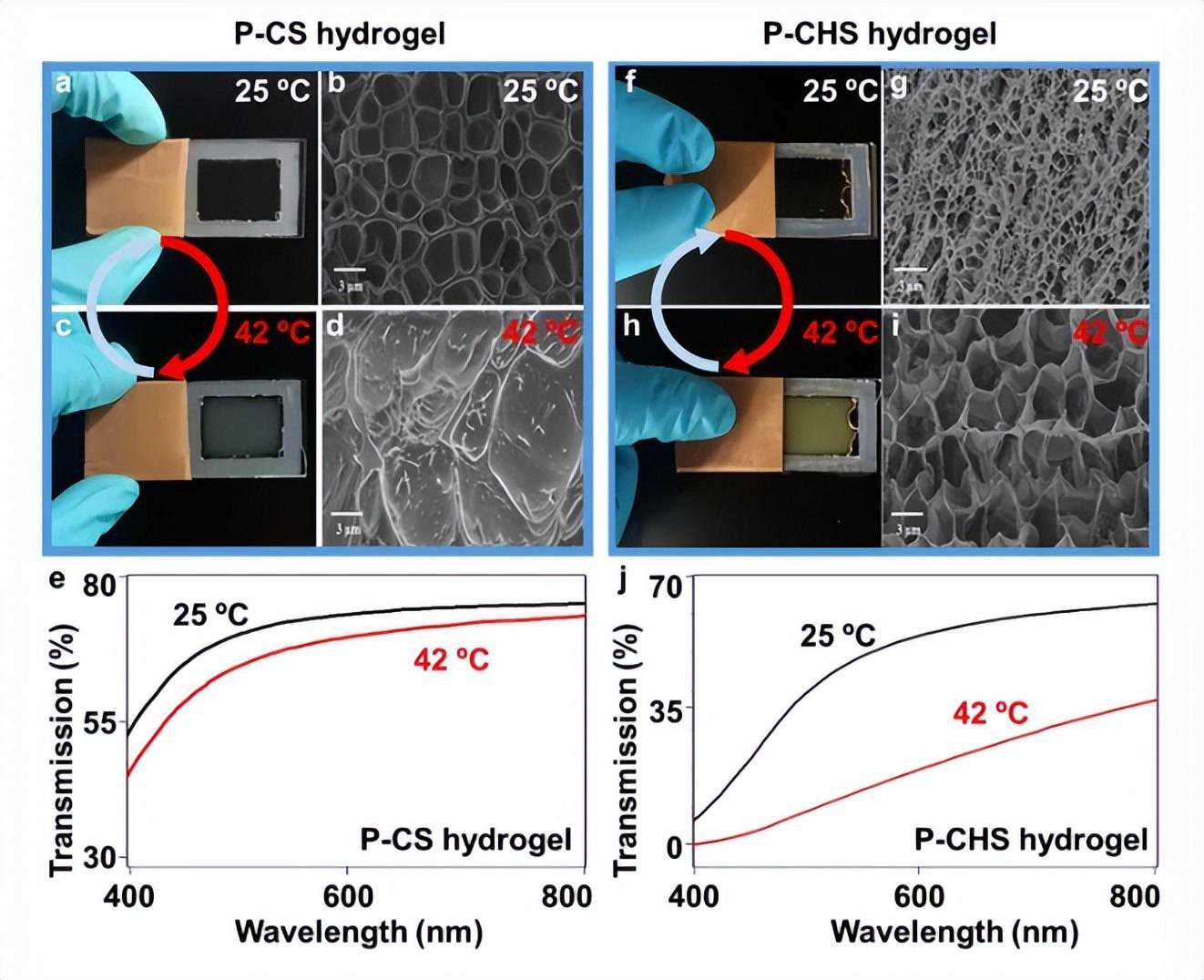
类似的程序也用于制备P-CHS水凝胶。P-CS和P-CHS水凝胶表现出易于可逆的热响应行为。通过将温度从25℃升高到42℃,水凝胶变得不透明,而可逆地降低温度则产生透明水凝胶。
根据扫描电子显微镜分析(SEM),冻干的P-CS水凝胶在25°C下含有均匀的多孔结构(2.5um)。
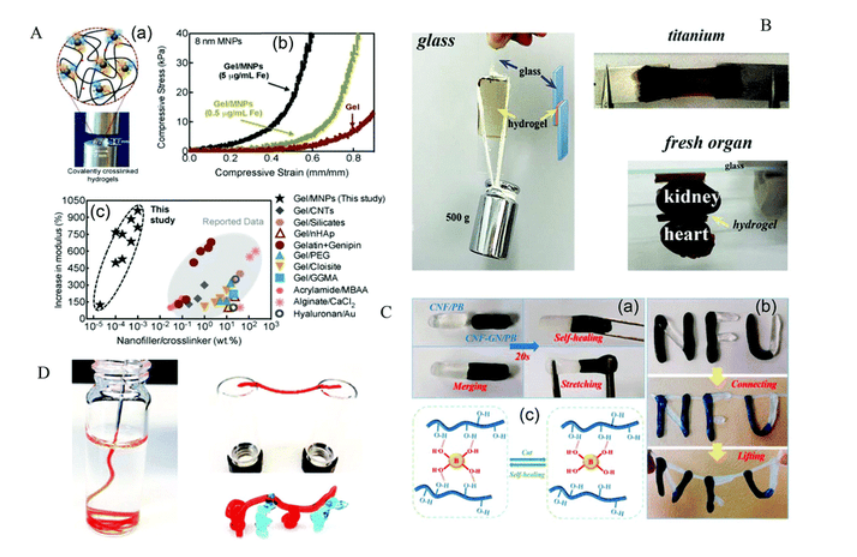
正如预期的那样,水凝胶在液氮中骤冷可能会导致小冰晶的形成,从而在样品快速冷却过程中诱导小孔的形成。
相比之下,42℃下冻干的P-CS水凝胶在冻干后仅显示出聚集结构。与P-CS水凝胶相比,25°C冷冻干燥的P-CHS水凝胶含有更小的孔隙(约1um)。当P-CHS水凝胶的温度从25℃升高到42℃时,孔变得更大(4um),并且没有表现出明显的塌陷聚集。
基于P-CS水凝胶和P-CHS水凝胶在25°C和42°C下可见光的透射率,还通过UV-vis分析证明了它们的光学性质。
首先,对照水凝胶没有表现出热响应特性。P-CS水凝胶在25℃下表现出良好的可见光透过率。
相比之下,P-CS水凝胶在42℃下的可见光透射率仅略有下降,例如,在600nm处从25℃到42℃下降了3%。
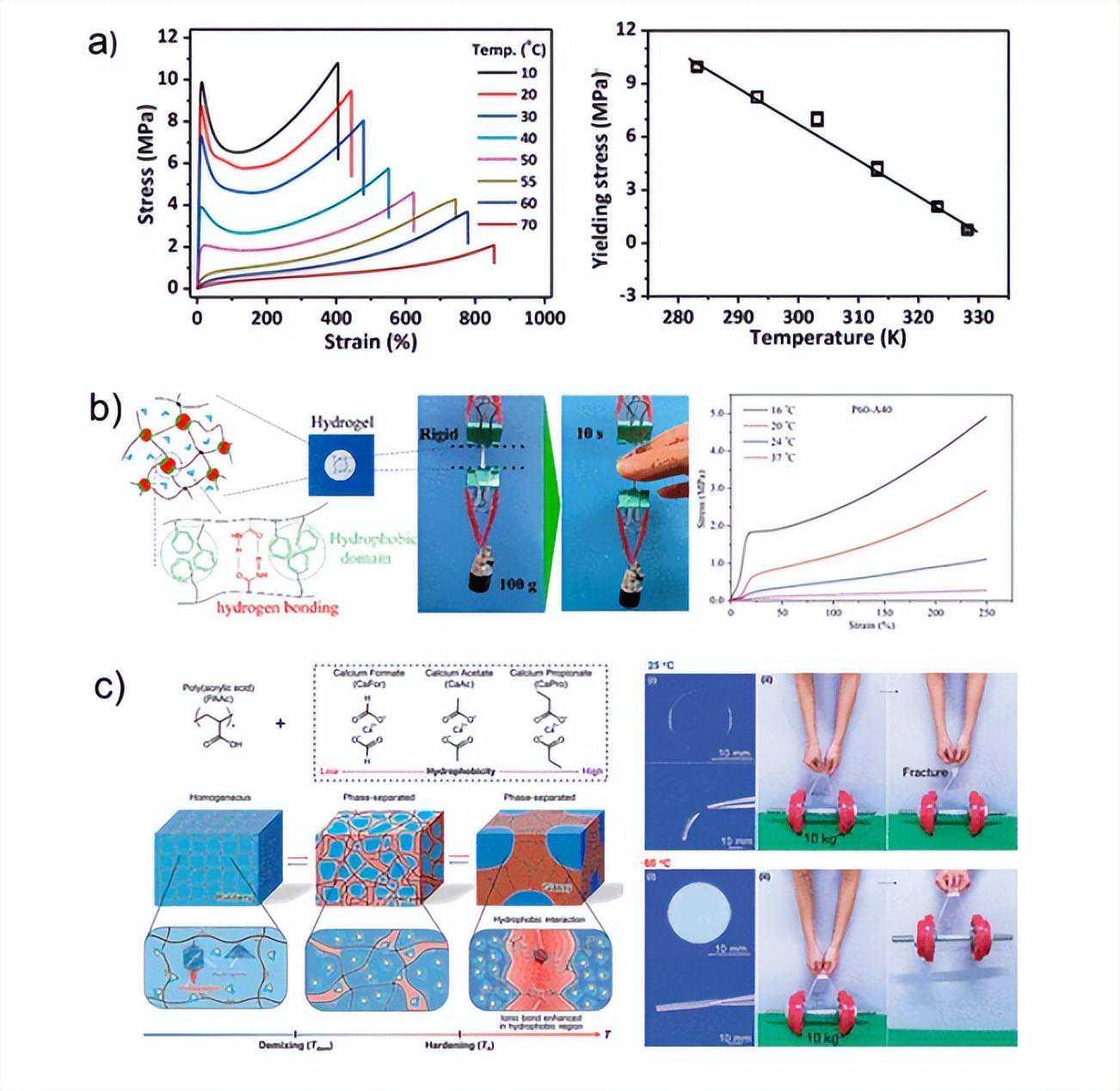
与P-CS水凝胶相比,P-CHS水凝胶在42°C下显着阻挡可见光的透射,例如,在600nm处从25°C到42°C减少了34%。
值得注意的是,P-CHS水凝胶由于其可见光透过率较低,在42°C下表现出比P-CS水凝胶更好的阻光性能。这可能是由于42°C时P-CHS中的聚集体分布比P-CS更不均匀所致。
通过对溶液中的聚合物进行DLS分析进一步证明了这一点。例如,虽然P-CS的流体动力学半径比P-CHS大10倍,但P-CS的PDI却是P-CHS的一半。观察到的P-CS水凝胶和P-CHS水凝胶的光学性质与P-CS和P-CHS水凝胶的热响应性质一致。
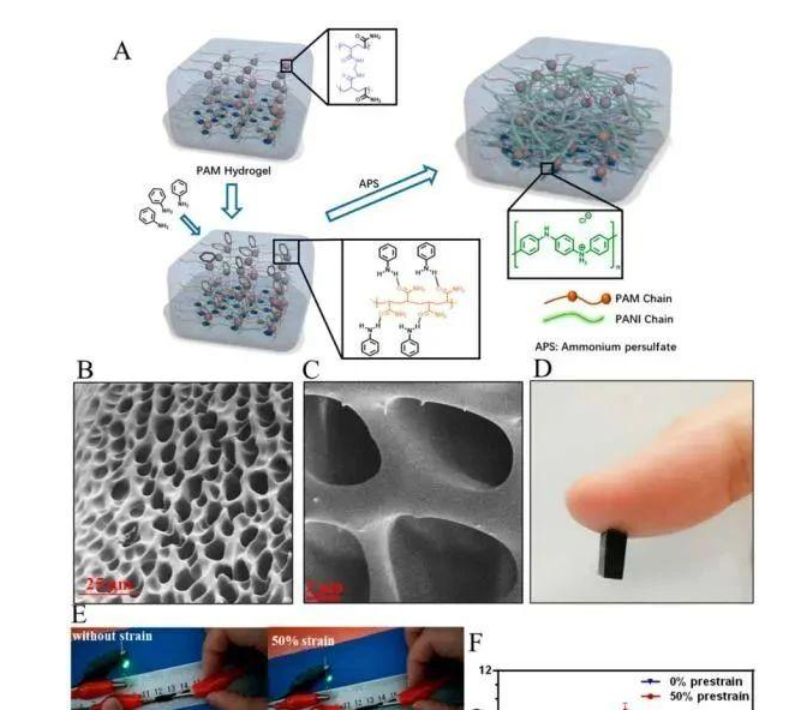
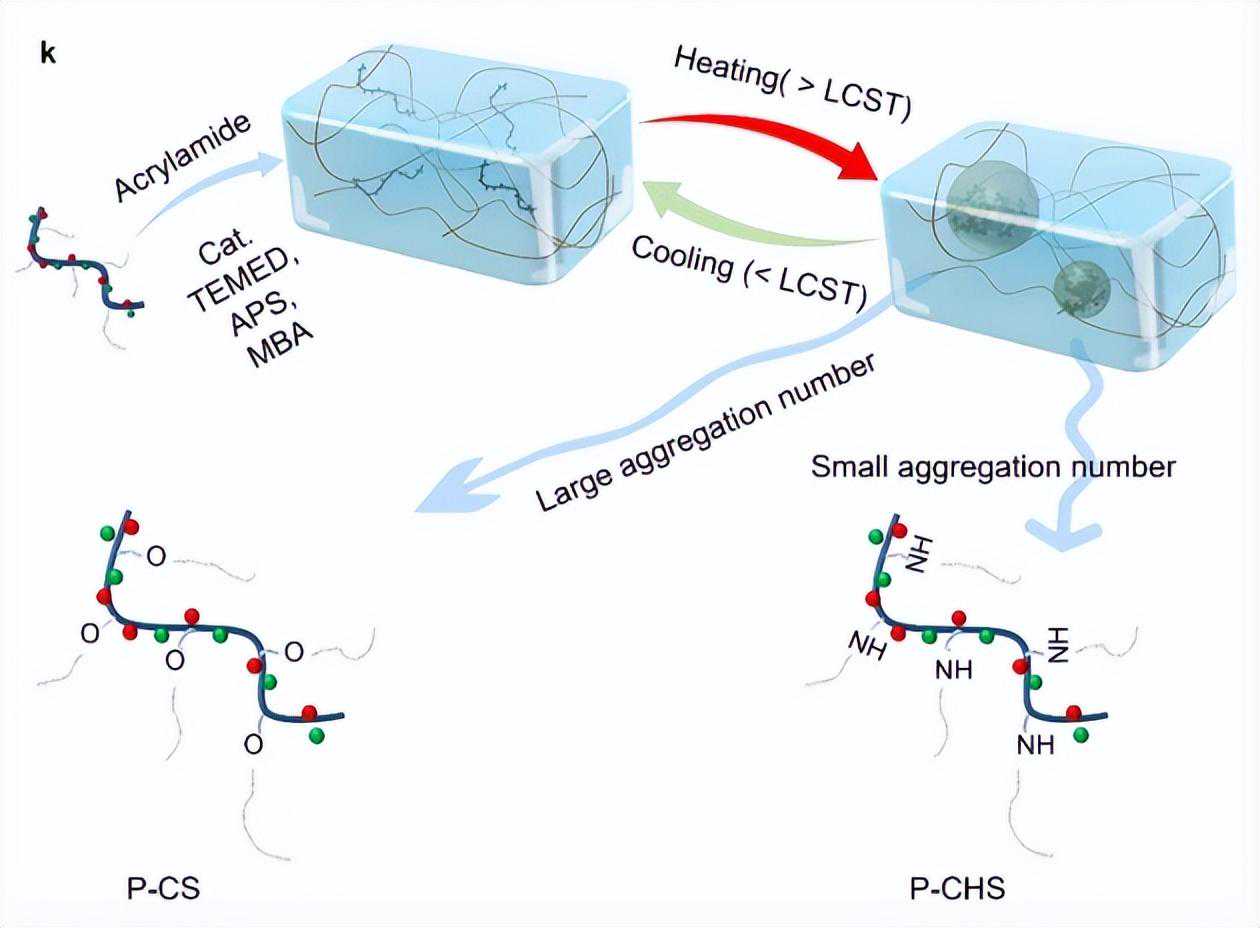
这些透明水凝胶不仅由于现有的PDMAEMA接枝在CS/CHS上而具有热响应性,离子多糖也可以很容易交联,使水凝胶网络对温度敏感。
在LCST以下,由于PDMAEMA的亲水链和水之间的分子间氢键,水凝胶具有透明的外观,这是基于离子P-CS/P-CHS的良好溶解性。P-CS/P-CHS的硫酸根和水分子之间的离子偶极力也有助于良好的溶解度。
将溶液温度提高到LCST以上后,由于聚合物链和水分子的破坏,出现了浊点,导致链逐渐折叠和热诱导聚集。
LCST行为通常是由聚合物的疏水域随温度变化而驱动的。此外,聚合物的亲水基团可以影响聚集体的形成及其尺寸。
具体而言,P-CS和P-CHS水凝胶之间的差异被证明主要归因于-O-和-NH-之间的碳水化合物主链差异。根据DLS结果和光学观察分析结果,与-O-相比,-NH-可以保持相对更好的亲水性,导致聚合物链的聚集尺寸更小,并且在较高温度下P-CHS水凝胶中表现出不均匀聚集。
相反,当温度升高时,-O-在P-CS水凝胶中诱导具有较低PDI的聚合物链的大聚集尺寸。
为了评估水和各种水凝胶之间的相互作用,对P-CHS和P-CS水凝胶的静态水接触角(SWCA)进行了表征。

CHS和P-CS水凝胶的SWCA相似,约为27°。这些结果表明P-CHS或P-CS水凝胶是亲水性的,并且P-CHS或P-CS聚合物的引入仅轻微影响这些水凝胶的亲水性。
为了评估P-CS和P-CHS水凝胶中不同碳水化合物主链对机械性能的影响,在25°C下记录了水凝胶的机械性能。
碳水化合物主链的结构和性质对具有硫酸化多糖衍生共聚物的热响应水凝胶的响应性能和机械性能具有重要影响。
通过深入研究和优化碳水化合物主链的选择和调控,可以实现水凝胶的性能调控和应用拓展,为生物医学领域和智能材料领域的发展提供新的可能性。













